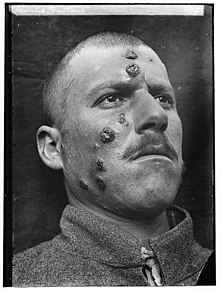
Leishmaniose é uma doença crônica, de manifestação cutânea ou visceral (pode-se falar de leishmanioses, no plural), causada por protozoários flagelados do gênero Leishmania, da família dos Trypanosomatidae. O calazar (leishmaniose visceral)[1] e a úlcera de Bauru (leishmaniose tegumentar americana)[2] são formas da doença.
 É uma zoonose comum ao cão e ao homem.[3] É transmitida ao homem pela picada de mosquitos flebotomíneos, que compreendem o gênero Lutzomyia (chamados de "mosquito palha" ou birigui) e Phlebotomus.
É uma zoonose comum ao cão e ao homem.[3] É transmitida ao homem pela picada de mosquitos flebotomíneos, que compreendem o gênero Lutzomyia (chamados de "mosquito palha" ou birigui) e Phlebotomus.No Brasil existem atualmente 6 espécies de Leishmania responsáveis pela doença humana, e mais de 200 espécies de flebotomíneos implicados em sua transmissão. Trata-se de uma doença que acompanha o homem desde tempos remotos e que tem apresentado, nos últimos 20 anos, um aumento do número de casos e ampliação de sua ocorrência geográfica, sendo encontrada atualmente em todos os Estados brasileiros, sob diferentes perfis epidemiológicos. Estima-se que, entre 1985 e 2003, ocorreram 523.975 casos autóctones, a sua maior parte nas regiões Nordeste e Norte do Brasil. Em Portugal existe principalmente a leishmaniose visceral e alguns casos (muito raros) de leishmaniose cutânea. Esta raridade é relativa, visto que na realidade o que ocorre é uma subnotificação dos casos de leishmaniose cutânea. Uma razão para esta subnotificação é o fato de a maioria dos casos de leishmaniose cutânea humana serem autolimitados, embora possam demorar até vários meses a resolverem-se.
As leishmania são transmitidas pelos insetos fêmeas dos gêneros Phlebotomus (Velho Mundo) ou Lutzomyia (Novo Mundo).
No início do século XX o médico paraense Gaspar Viana iniciou estudos sobre a leishmaniose, e a ele atribui-se a descoberta dos primeiros tratamentos para a doença. A doença também pode afetar o cão ou a raposa, que são considerados os reservatórios da doença, conforme referido pelo médico sanitarista Thomaz Corrêa Aragão, em 1954.
As leishmania são protozoários parasitas de células fagocitárias de mamíferos, especialmente de macrófagos. São capazes de resistir à destruição após a fagocitose. As formas promastigotas (infecciosas) são alongadas e possuem um flagelo locomotor anterior, que utilizam nas fases extracelulares do seu ciclo de vida. O amastigota (intra-celular) não tem flagelo.
Há cerca de 30 espécies patogênicas para o ser humano (CDC). As mais importantes são:
- As espécies L. donovani, L. infantum infantum, e L. infantum chagasi que podem produzir a leishmaniose visceral, mas, em casos leves, apenas manifestações cutâneas.
- As espécies L. major, L. tropica, L. aethiopica, L. mexicana, L. braziliensis, L. amazonensis e L. peruviana que produzem a leishmaniose cutânea ou a mais grave, mucocutânea.
Ciclo de vida
O ciclo de vida das espécies é ligeiramente diferente mas há pontos comuns. São libertados no sangue junto com a saliva de flebotomíneos ou flebótomos (em inglês são denominados sand flies) no momento da picada. As leishmanias na forma de promastigotas ligam-se por receptores específicos aos macrófagos, pelos quais são fagocitadas. Elas são imunes aos ácidos e enzimas dos lisossomas com que os macrófagos tentam digeri-las, e transformam-se nas formas amastigotas após algumas horas (cerca de 12h). Então começam a multiplicar-se por divisão binária, saindo para o sangue ou linfa por exocitose e por fim conduzem à destruição da célula, invadindo mais macrófagos. Os amastigotas ingeridos pelos insectos transmissores demoram oito dias ou mais a transformarem-se em promastigotas e multiplicarem-se no seu intestino, migrando depois para as probóscides.Leishmaniose visceral
LV Humana
Em hospedeiros humanos, a resposta da infecção por L. donovani varia bastante, não só pela força mas também pelo tipo da reação imune do paciente. Pacientes que produzem números grandes de células-T do tipo TH1, que ativa a resposta celular mas não encorajam a formação de anticorpos, frequentemente recuperam-se da infecção e depois são imunes a uma reinfecção. Pacientes cujos sistemas produzem mais células do tipo TH2, que promovem apenas a formação de anticorpos, são mais afetados.
W -enciclopédia livre
Na leishmaniose visceral humana, os primeiros sintomas podem ser
associados ao descamamento da pele - com destaque para regiões em torno
do nariz, boca, queixo e orelhas, sendo frequentes também no couro cabeludo, onde estes são geralmente confundidos com caspa;
e ao aparecimento de pequenos calombos semiesféricos sob o couro
cabeludo, geralmente sensíveis ao toque. Tais calombos surgem e
desaparecem com frequência sem contudo implicarem, de forma geral mas
não restritiva, feridas. Não obstante, por incômodo, estes podem evoluir
para lesões mediante traumas induzidos pelas unhas ou mãos do próprio
paciente; tais lesões geralmente cicatrizam-se, contudo, de forma
normal. Alterações nos níveis de ácido úrico que não associam-se adequadamente às causas típicas desta anomalia - a exemplo bem notórias mesmo em pacientes vegetarianos - e que acabam por implicar sintomas muito semelhantes aos da gota - bem como alterações na quantificação de enzimas associadas ao fígado - como a gama glutamil transferase e transaminase pirúvica - passam a ser detectáveis em exames de sangue. Com a evolução da doença os sintomas mais típicos incluem o aumento do baço ou esplenomegalia, sendo este geralmente também acompanhado do aumento do fígado ou hepatomegalia, ambos detectáveis via ultrassonografia.
Se deixado sem tratamento a doença evolui para um quadro crítico
caracterizado por rápido e intenso emagrecimento, dor abdominal,
ausência de apetite, apatia e febre
alta, intermitente e crônica - com duração superior a dez dias - fase
na qual o paciente geralmente é levado a procurar o médico. Nesta fase
os hemogramas geralmente revelam, entre outras anomalias, os níveis de albumina e contagem de leucócitos significativamente alterados, sendo notórias a anemia e a leucopenia.
A mortalidade da doença nesta etapa é consideravelmente aumentada por
estes sintomas serem facilmente confundidos com os de outras patogenias;
nesta fase, se deixada sem tratamento, a doença quase sempre implica a
morte do paciente. O escurecimento da pele, que deu à doença seu nome comum na Índia, não aparece na maioria dos casos de doença, e os outros sintomas são muito fáceis de confundir com os da malária. O erro no diagnóstico é perigoso, pois, sem tratamento, a taxa de mortalidade para kala-azar está próxima a 100%.Humanos e outros animais infectados são considerados reservatórios da doença, uma vez que o mosquito, ao sugar o sangue destes, pode transmiti-lo a outros indivíduos ao picá-los. Em região rural e de mata, os roedores e raposas são os principais; no ambiente urbano, os cães. Nem todos os cães, quando infectados, apresentam os sinais da doença (emagrecimento, perda de pelos e lesões na pele).
Algum tempo depois do tratamento pode surgir uma forma secundária da [doença], chamada leishmaniose dérmica pós-kala-azar ou LDPK. Esta condição se manifesta primeiro como lesões de pele na face que gradualmente aumentam em tamanho e espalham-se pelo corpo. Eventualmente as lesões podem ser desfigurantes, deixando cicatrizes semelhantes a lepra e causando cegueira ocasionalmente se atingirem os olhos: contudo a doença não é a leishmaniose cutânea, mas uma doença causada por outro protozoário do gênero Leishmania, que também afeta neste estágio a pele.
LV Canina

Leishmaniose cutânea
Leishmaniose mucocutânea
O tratamento para a leishmaniose mucocutânea é a combinação de pentoxifilina e um antimônio pentavalente em dosagens altas durante 30 dias: isto alcança taxas de cura de 90%. Tratamento só com antimônio pentavalente não cura 42% dos pacientes, até mesmo naqueles que alcançam uma cura aparente, 19% recairá.
Transmissão

Mosquito flebotomíneo
Se, pouco depois de infectar-se, o flebotomíneo volta a alimentar-se com sangue, o crescimento dos flagelados pode ser inibido. Mas se a segunda refeição for feita com sucos de plantas (ou, nas condições de laboratório, com passas ou soluções açucaradas), as formas promastigotas multiplicar-se-ão abundantemente no tubo digestivo do inseto. Quando ele ingere novamente sangue, poderá regurgitar com o sangue aspirado grumos de leishmanias (promastigotas infectantes) que cresciam no esôfago e no proventrículo.
Em vista do tempo requerido para o crescimento abundante dos flagelados e da vida curta dos insetos adultos (cerca de duas semanas ou pouco mais), é necessário que o flebotomíneo se infecte muito cedo, talvez por ocasião de suas primeiras refeições sanguíneas, para que possa efetuar a transmissão do calazar.
A proporção de insetos encontrados com infecção natural é sempre muito baixa. Assim, a transmissão fica na dependência de existir, nos focos americanos, uma densidade grande de Lutzomyia longipalpis, fato que se constata nas áreas de leishmaniose visceral, mesmo no interior das casas, sempre que haja um surto epidêmico.
Outro mecanismo de transmissão possível, entre os animais, é a transmissão direta, sem flebotomíneos. Em certas áreas endêmicas, observou-se a pequena densidade de insetos vetores, raros casos humanos e grande incidência do calazar canino. Como os flebotomíneos aí mostravam poucas tendências em picar os cães, supôs-se que a propagação pudesse ter lugar por contato sexual, tanto mais que em diversas pesquisas pôde-se comprovar o parasitismo da glande e da uretra dos cães por leishmanias.

- Leishmaniose principalmente visceral (organismos mais agressivos):
- A L. donovani é a mais frequente causa de leishmaniose visceral. Em algumas regiões (Índia Paquistão, Bangladesh e Sudão) encontra-se uma forma de leishmaniose dérmica pos-kalazar (PKDL). É transmitida por Phlebotomus e existe no subcontinente indiano e na África equatorial (rara em Angola e Moçambique). O reservatório são os seres humanos e os cães.
-
- A L. infantum infantum provoca uma variante menos grave da leishmaniose visceral e existe na região mediterrânica, incluindo países do Norte de África, Turquia, Israel, Grécia, Itália, sul da França, Portugal e Espanha e ainda nos Balcãs, Irão, algumas regiões da China e Ásia central. É transmitida pelo Phlebotomus e o seu reservatório são os cães, lobos e raposas. Em Portugal é mais frequente em regiões como Trás-os-Montes, Coimbra e a Beira Litoral, Algarve e na região dos estuários dos rios Sado e Tejo.
-
- A L. infantum chagasi existe na América Latina, incluindo Brasil. O inseto transmissor é o flebotomíneo Lutzomyia. Reservatórios: cães e gambás. Esta espécie é considerada uma subespécie de L. infantum.
- Leishmaniose principalmente cutânea (organismos de virulência baixa):
- L. major: Norte de África, Médio Oriente e Ásia Central. Transmitida por Phlebotomus. Reservatório: roedores. Responsável por produzir ulcerações úmidas, de evolução rápida.
-
- L. aethiopica: Existe na Etiópia e no Quénia. Transmitida por Phlebotomus. Reservatório: Hyrax, espécies de pequenos mamíferos.
-
- L. tropica: Existe em países da costa Sul e Leste do Mediterrâneo e no Médio Oriente. Transmitida por Phlebotomus. O reservatório é principalmente humano (antroponose), mas o Hyrax também foi incriminado em alguns foci.
-
- L. mexicana: encontra-se no México, na Guatemala e Belize. Transmissão pelo Lutzomyia. O reservatório são os roedores e marsupiais. Gera úlceras benignas na pele.
-
- L. amazonensis: América do Sul. Transmissão pelo Lutzomyia. O reservatório são os roedores. Produz lesões cutâneas, às vezes múltiplas.
- Leishmaniose principalmente mucocutânea (virulência intermédia):
- L. braziliensis: existe em todo o Brasil, Venezuela, Colômbia e Guianas. Lutzomyia. Reservatório: roedores e gambás. Caracteriza-se por formar úlceras cutâneas (raramente múltiplas), expansivas e persistentes, frequentemente acompanhadas de lesões graves da nasofaringe.
-
- L.peruviana: predomina nos países andinos, Bolívia, Peru, Equador, Colômbia e Venezuela. Reservatório: cães.
Prevalência
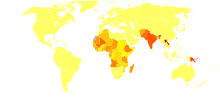
Estima-se que a Leishmaniose (tegumentar e visceral) no ano de 2003 apresentava uma prevalência de 12 milhões de casos no mundo e que 350 milhões de pessoas viviam nas áreas com risco de contrair a doença. Segundo a OMS, 2 milhões de pessoas são contaminadas todos os anos (1,5 milhões de casos de leishmaniose cutânea e 500 000 casos de leishmaniose visceral). E esse número parece estar aumentando.[5]
Essa doença está espalhada por 88 países, dos quais 72 são países em desenvolvimento. A grande maioria dos casos de Leishmaniose visceral ocorrem no Brasil, Bangladesh, Índia ou Sudão. A grande maioria dos casos de leishmaniose cutâneo-mucosa ocorrem no Brasil, Bolívia ou Peru. E a maioria dos casos de leishmaniose cutânea ocorrem no Brasil, Afeganistão, Irã, Peru, Arábia Saudita ou Síria. Mais de 90% dos casos ocorrem nesses países, sendo o Brasil o único a reunir grandes números de casos dos 3 tipos de leishmaniose.
Os casos são mais comuns nas áreas de criação de gado onde os animais também são vítimas da doença e ocorrem contaminações cruzadas (do homem para o animal e do animal para o homem).
Progressão e sintomas
Uma infecção por leishmanias pode tomar dois cursos. Na maioria dos casos o sistema imunitário reage eficazmente pela produção de uma resposta citotóxica (resposta Th1) que destrói os macrófagos portadores de leishmanias. Nestes casos a infecção é controlada e os sintomas leves ou inexistentes, curando-se o doente ou desenvolvendo apenas manifestações cutâneas. No entanto, se o sistema imunitário escolher antes uma resposta (humoral ou Th2) com produção de anticorpos, não será eficaz a destruir as leishmanias que se escondem no interior dos macrófagos, fora do alcance dos anticorpos. Nestes casos a infecção (apenas L. donovani irá se desenvolver em leishmaniose visceral), uma doença grave, ou no caso das espécies menos virulentas, para manifestações mucocutâneas mais agressivas e crónicas. Um indivíduo imunodeprimido não reage com nenhuma resposta imunitária eficaz, e estes, especialmente os doentes com SIDA/AIDS, desenvolvem progressões muito mais perigosas e rápidas com qualquer dos patogénios. Em Portugal, Espanha, Itália e França este grupo tem ultimamente formado uma percentagem grande dos doentes com formas de leishmaniose graves.A leishmaniose visceral, também conhecida por kala-azar ou febre dumdum, tem um período de incubação de vários meses a vários anos. As leishmanias danificam os órgãos ricos em macrófagos, como o baço, o fígado, e a medula óssea. Os sintomas mais comuns do kala azar são[6]:
- Febre prolongada,
- Úlceras escuras na pele
- Aumento do baço (esplenomegalia),
- Aumento do fígado (hepatomegalia),
- Leucopenia,
- Anemia,
- Hipergamaglobulinemia,
- Tosse,
- Dor abdominal,
- Diarréia,
- Perda de peso e;
- caquexia.
A leishmaniose cutânea tem uma incubação de algumas semanas a alguns meses (geralmente) assintomáticos, após o qual surgem sintomas como lesões na pele (pápulas ulcerantes) extremamente irritantes nas zonas picadas pelo mosquito, que progridem para crostas com líquido seroso. Há também escurecimento por hiperpigmentação da pele, com resolução das lesões em alguns meses com formação de cicatrizes desagradáveis. A leishmaniose mucocutânea é semelhante mas com maiores e mais profundas lesões, que se estendem às mucosas da boca, nariz ou genitais.
Áreas endêmicas no Brasil
No Brasil, o maior número de casos são registrados nas regiões Norte e Nordeste, onde a precariedade das condições sanitárias favorecem a propagação da doença. Mas o aumento do número de registros na Região Sudeste mostram que todo o país corre risco de epidemias de Leishmaniose. O interior paulista tem assistido a um crescimento grande do número de casos. Em 1999, Araçatuba enfrentou uma epidemia. Birigui e Andradina também registraram alto número de casos da doença. Em 2003, Bauru passou a registrar a doença de forma endêmica. Em todas essas cidades ocorreram óbitos, e há o risco da doença chegar a grandes centros urbanos paulistas de forma endêmica, como Campinas, Sorocaba, Santos e São Paulo.Em Campo Grande, capital sul-matogrossense, a incidência da doença também é alta, principalmente em cães que são frequentemente recolhidos pelo poder público e submetidos a eutanásia. Tal atitude tenta conter a doença na cidade, mas nada é feito quanto ao combate efetivo do mosquito transmissor.
Segundo dados da Secretaria Municipal de Saúde de Corumbá, em 2006, 52,43% dos cães da cidade tiveram diagnóstico positivo para leishmaniose visceral. Em 2004, eram 41,63%, demonstrando um crescimento significativo.[7]
A leishmaniose é considerada pela DNDi como uma doença "extremamente negligenciada", assim como a doença do sono e a de doença de Chagas. Isto porque, em razão da prevalência em regiões de extrema pobreza, não há interesse por parte da indústria farmacêutica em desenvolver novos medicamentos para essas doenças.
Prevenção, diagnóstico e tratamento
O diagnóstico é pela observação directa microscópica dos parasitas em amostras de linfa, sanguíneas ou de biópsias de baço, após cultura ou por detecção do seu DNA ou através de testes imunológicos, como a Reação de Montenegro.O tratamento humano é feito por administração de compostos de antimónio, pentamidina, marbofloxacino anfotericina ou miltefosina. Deve-se muito ao pesquisador Gaspar Vianna, auxiliar de Carlos Chagas, ao se falar em tratamento para as leishmanioses.
A prevenção se faz por redes ou repelentes de insectos, pela construção de moradias humanas a distância superior a 500 metros da mata silvestre e pela erradicação dos Phlebotomus/Lutzomyia. Um importante e por muitos um controverso ponto no controle da leishmaniose reside na redução dos reservatórios da doença via eutanásia dos animais domésticos diagnosticados como portadores da doença. As prefeituras de localidades com presença significativa desta patologia geralmente mantêm serviços de patrulha e diagnóstico de animais de estimação infectados, determinando que setor de controle de zoonoses associado realize periodicamente exames de sangue gratuitos nos animais de estimação, e que este recolha e proceda a eutanásia de animais soropositivos.
Embora os agentes do serviço de controle de zoonoses geralmente cumpram com regularidade as atividades que lhe são incumbidas, ressalva significativa é feita quanto ao fato de que estes (quase?) nunca encaminham, ou sequer aconselham, os moradores da residência associada a um animal positivo-diagnosticado a também realizarem os exames diagnósticos associados. Aparte os motivos de tal atitude, os exames são geralmente simples, rápidos e baratos. Mostram-se acessíveis a todos via postos de saúde públicos ou mesmo na rede particular, e devem ser feitos por todos os moradores da residência onde haja o diagnóstico de um animal com a doença. Até o ponto em que se sabe - contradizendo as estatísticas divulgadas na mídia de enorme número de casos em animais e poucos em humanos - tanto homens quanto os cachorros, gatos, e demais mamíferos do ambiente doméstico - como ratos - estão igualmente suscetíveis à contaminação.
Entre as moléculas mais utilizadas no tratamento da leishmaniose canina estão os antimoniais e o alopurinol.
Vacina
A vacina terapêutica para leishmaniose, desenvolvida pelo Prof. Wilson Mayrink, pesquisador do Departamento de Parasitologia da Universidade Federal de Minas Gerais, recebeu o registro do Ministério da Saúde e agora pode ser comercializada no Brasil.[8][9][10] Segundo o Prof. Mayrink, a vacina está sendo testada na Colômbia e no Equador, sob a coordenação da OMS. Os testes estão em fase final e, até agora, os resultados são semelhantes aos do Brasil. O pesquisador está otimista também com os resultados dos testes da vacina preventiva, realizados nos municípios de Caratinga e Varzelândia, em Minas Gerais. Ele acredita que, nos próximos dois anos, a vacina preventiva também possa ser produzida em escala industrial e comercializada em todo o País.No cão ainda não existe uma vacina comercializada na Europa. Atualmente a forma mais eficaz de prevenção passa pela utilização de produtos especiais com efeito de repelência sobre os flebótomos. Estão comercializados vários produtos à base de piretróides sintéticos. O produto que tem demonstrado maior eficácia, sendo o mais recomendado e referenciado, é a coleira impregnada com deltametrina. Em maio de 2007, as autoridades sanitárias do Município de Campo Grande, Mato Grosso do Sul, adquiriram vários milhares destas coleiras para fazer frente à leishmaniose canina.
Creditos e Direitos Autorais .Wikipedia .Enciclopédia livre